宝剑锋从磨砺出,梅花香自苦寒来,杰华生物技术(青岛)有限公司于2016年5月20日从北京中试基地接收工程菌,5月26日开始进行第一轮工艺放大:发酵规模放大到300L、纯化规模每批放大到2kg,比中试规模放大10倍。公司广大参与人员与中试技术人员并肩作战,协调配合,至6月4日完成全部的原液制备工作。经过初步质量检测:原液蛋白浓度、电泳纯度、内毒素含量、反相纯度、分子筛纯度和生物活性等几项主要指标均符合质量标准,其中相关蛋白含量仅为3.2%,优于欧盟标准。
按照常规做法和行业经验,生物制药厂的建设及认证周期需要3年时间。杰华项目从去年8月1日到今年6月1日刚刚10个月,在保证安全、质量的前提下,现已高标准完成项目工程的全部建设,完成了设备的安装、调试、验证、工艺放大等相关工作,初步具备了试生产的相关条件!这是杰华团队努力拼搏、奋发图强的结果,是政府关怀,广大的现场工程施工人员,设备供应商高度协调配合,精诚团结夜以继日共同努力的产物。
我们将发扬连续作战的作风,力争年底通过GMP认证,产品正式上市。我们共同在书写传奇,为“青岛速度”注入真正的内涵!

生产厂房外貌

工艺放大技术团队
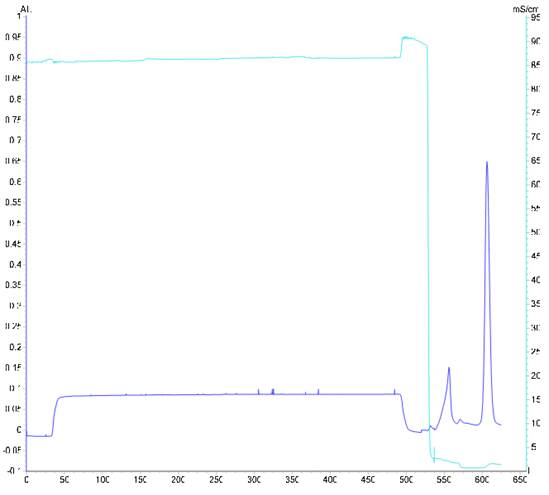
蛋白纯化层析图谱

发酵菌体蛋白表达电泳图谱